El ensayo cuantitativo de suspensión es una metodología utilizada para medir la capacidad de un producto desinfectante o antiséptico para reducir la cantidad de bacterias viables en una suspensión líquida bajo condiciones específicas. Este método es fundamental para asegurar que los productos cumplan con los requisitos de eficacia necesarios para su uso seguro y efectivo. En este artículo, se compararán varios aspectos clave de estas normas, incluyendo su campo de aplicación, las condiciones de ensayo, los organismos de ensayo utilizados, los requisitos mínimos de reducción logarítmica y los procedimientos de validación. A través de esta comparación, se busca proporcionar una visión clara y comprensible de las similitudes y diferencias entre estas importantes normas.
Ensayo Cuantitativo de Suspensión para Desinfectantes
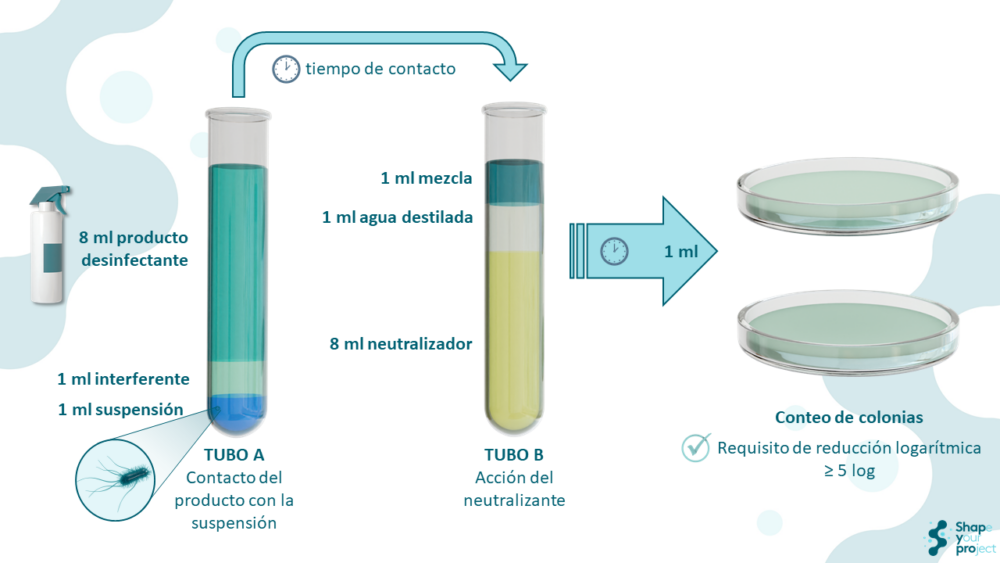
El ensayo cuantitativo de suspensión es una técnica de laboratorio diseñada para evaluar la efectividad biocida de productos antisépticos y desinfectantes. Consiste en añadir una cantidad específica del producto a una suspensión de bacterias y, después de un tiempo de contacto definido, neutralizar la acción del desinfectante y determinar la cantidad de bacterias que han sobrevivido. Este método es crucial porque simula condiciones prácticas de uso y proporciona datos cuantitativos sobre la capacidad del producto para reducir la carga bacteriana.
Las condiciones de ensayo incluyen factores como la temperatura, el tiempo de contacto y la presencia de sustancias interferentes. Estos factores se seleccionan para reflejar las condiciones en las que se utilizarán los productos en la práctica. Las sustancias interferentes, como la albúmina bovina y la leche, se utilizan para simular la presencia de materia orgánica que podría afectar la efectividad del desinfectante.
Campo de Aplicación
Las normas EN 1656:2019, EN 1276:2019 y EN 13727:2012+A2:2015 se aplican en diferentes contextos, aunque todas comparten el objetivo de evaluar la eficacia bactericida de desinfectantes y antisépticos químicos. La EN 1656:2019 se centra en la evaluación de la actividad bactericida de productos utilizados en el área veterinaria. Por otro lado, la EN 1276:2019 evalúa la actividad bactericida en áreas alimentarias, industriales, domésticas e institucionales, mientras que la EN 13727:2012+A2:2015 está diseñada específicamente para el área médica, evaluando la actividad bactericida de productos utilizados en la desinfección de superficies, manos y equipos médicos.
Condiciones de Ensayo
Las condiciones de ensayo descritas en las normas son fundamentales para asegurar que los resultados sean comparables y reproducibles. Las normas especifican condiciones limpias y sucias.
Las condiciones limpias simulan situaciones donde la superficie a desinfectar no está significativamente contaminada con materia orgánica. En la norma EN 1276:2019, se utiliza una solución de albúmina bovina al 0,3 g/l, que representa niveles bajos de proteínas que podrían interferir con la acción del desinfectante. Por otro lado, las condiciones sucias simulan situaciones más desafiantes, donde hay una mayor cantidad de materia orgánica presente. En estos casos, se usa una solución de albúmina bovina al 3 g/l, lo que representa un entorno más contaminado que puede dificultar la efectividad del desinfectante. Las normas contemplan la inclusión de sustancias interferentes adicionales relevantes según el campo de aplicación específico, tales como diferentes proteínas, lípidos, y detergentes.
En contextos alimentarios también se especifica el uso de leche reconstituida al 1% (v/v) como sustancia interferente en ciertos ensayos. La leche es relevante en el contexto del procesamiento de alimentos, ya que representa residuos de productos lácteos que pueden encontrarse en equipos y superficies de procesamiento. Utilizar leche en los ensayos asegura que los desinfectantes sean efectivos en condiciones que imiten mejor las situaciones reales en la industria alimentaria. Para preparar esta solución, se reconstituye leche descremada garantizada exenta de antibióticos y aditivos, con 100 g de leche en polvo por litro de agua, calentándola a altas temperaturas.
En la norma EN 1656:2019, se describen condiciones de suciedad a dos niveles: bajo, utilizando una solución de albúmina bovina al 3 g/l, y alto, combinando una solución de albúmina bovina al 10 g/l con extracto de levadura al 10 g/l.
Por otro lado, la EN 13727:2012+A2:2015 detalla condiciones específicas para el área médica, incluyendo el uso de albúmina bovina y eritrocitos como sustancias interferentes. Para simular condiciones sucias en ensayos médicos, se utiliza una solución de albúmina bovina a 3 g/l mezclada con 3 ml/l de eritrocitos, reflejando la presencia de sangre y otras proteínas en el entorno clínico. Estas condiciones aseguran que los productos sean evaluados de manera que se refleje su efectividad en situaciones prácticas de uso hospitalario, donde la eliminación de patógenos es crítica para la prevención de infecciones nosocomiales.
Organismos de Ensayo
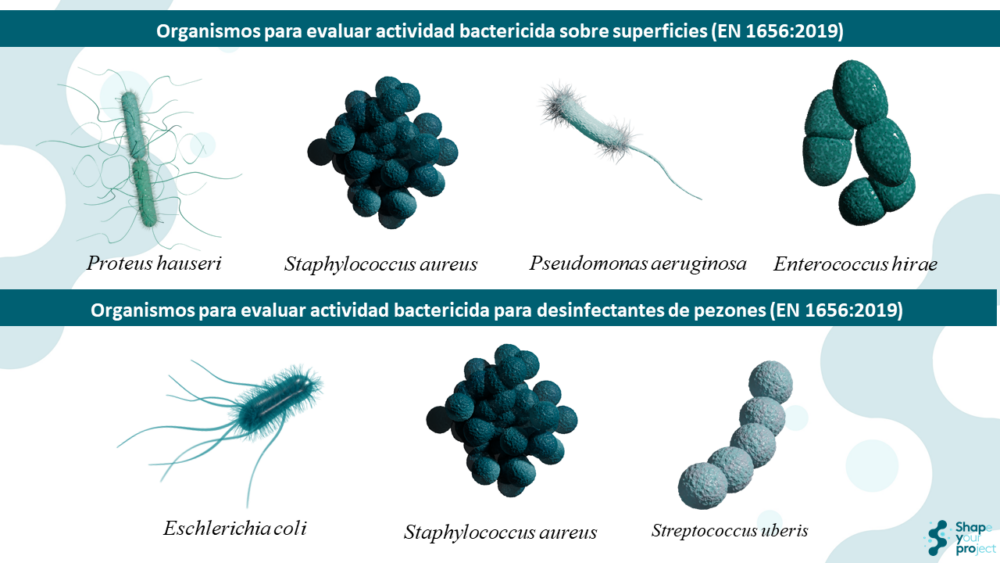
Los organismos de ensayo utilizados en estas normas varían según el campo de aplicación de la norma.
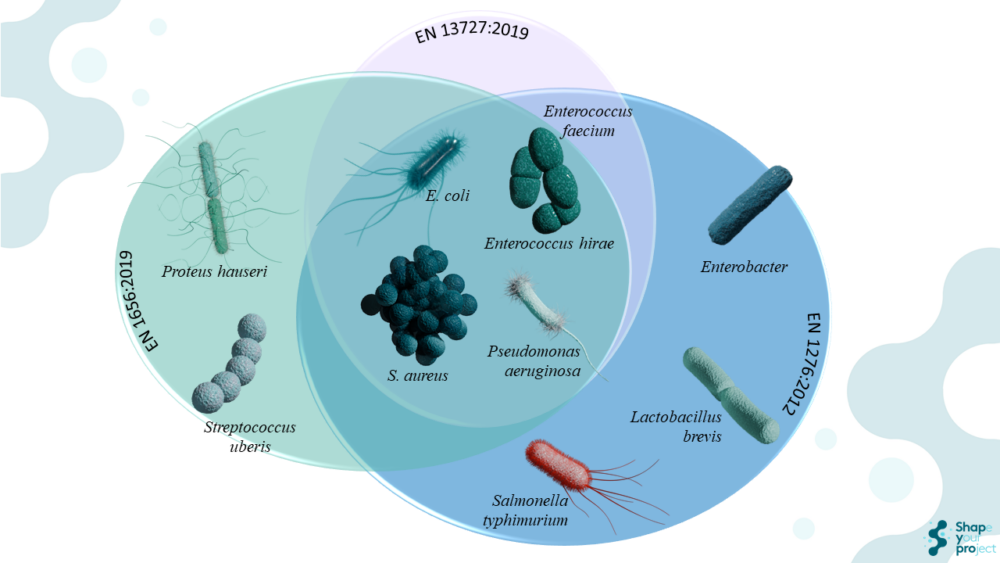
En la EN 1656:2019, se emplean cepas bacterianas específicas como Enterococcus hirae ATCC 10541, Proteus hauseri ATCC 13315, Pseudomonas aeruginosa ATCC 15442 y Staphylococcus aureus ATCC 6538 para productos de desinfección general. Para desinfectantes de pezones, se utilizan Escherichia coli ATCC 10536, Staphylococcus aureus ATCC 6538 y Streptococcus uberis ATCC 19436. Enterococcus hirae es una bacteria grampositiva que se utiliza como organismo de prueba debido a su resistencia intrínseca a muchos agentes antimicrobianos. Proteus hauseri, anteriormente conocido como Proteus vulgaris, es una bacteria gramnegativa relevante en el ámbito veterinario. Pseudomonas aeruginosa es una bacteria gramnegativa conocida por causar infecciones en individuos inmunocomprometidos y su resistencia a desinfectantes. Staphylococcus aureus es una bacteria grampositiva que causa diversas infecciones, incluyendo infecciones cutáneas y neumonía. Escherichia coli es una bacteria gramnegativa que se encuentra en el intestino humano y animal. Streptococcus uberis es una bacteria grampositiva relevante en infecciones mamarias en el ámbito veterinario.
La EN 1276:2019, por otro lado, se enfoca en cepas bacterianas específicas como Pseudomonas aeruginosa ATCC 15442, Escherichia coli ATCC 10536, Staphylococcus aureus ATCC 6538 y Enterococcus hirae ATCC 10541. Adicionalmente, se pueden emplear Salmonella Typhimurium ATCC 13311, Lactobacillus brevis DSM 6235 y Enterobacter cloacae DSM 6234 para aplicaciones específicas. Para temperaturas superiores a 40 °C, se debe emplear Enterococcus faecium ATCC 6057.
En el caso de la EN 13727:2012+A2:2015, se utilizan cepas bacterianas relevantes en el contexto médico, incluyendo Pseudomonas aeruginosa ATCC 15442, Staphylococcus aureus ATCC 6538, Escherichia coli K12 NCTC 10538, Enterococcus hirae ATCC 10541 y Enterococcus faecium ATCC 6057. La elección de estos organismos se debe a su relevancia clínica y su resistencia a los desinfectantes, lo que asegura que los productos sean efectivos contra los patógenos que más comúnmente causan infecciones nosocomiales.
Si se utilizan organismos de ensayo adicionales, deben incubarse bajo las condiciones óptimas de crecimiento especificadas en el informe de ensayo, incluyendo temperatura, tiempo, atmósfera y medio. Estos organismos adicionales deben ser verificados para asegurar su idoneidad y, si no están clasificados en un centro de referencia, deben ser caracterizados adecuadamente. Además, el laboratorio de ensayo o el banco nacional de cultivos debe mantener estos organismos como referencia durante un período de cinco años.
Requisitos Mínimos de Reducción Logarítmica y Procedimientos de Validación
Las normas establecen requisitos mínimos de reducción logarítmica para asegurar que los productos sean efectivamente biocidas. La reducción logarítmica es una medida de la disminución en el número de microorganismos viables después del tratamiento con un desinfectante.
En la norma EN 1656:2019, se requiere que los productos logren una reducción de al menos 5 logaritmos decimales en condiciones sucias de nivel bajo simuladas (solución 3 g/l de albúmina bovina) o condiciones sucias de nivel alto simuladas (solución 10 g/l de solución albúmina bovina y 10 g/l de extracto de levadura). Para desinfectantes de pezones, la reducción mínima requerida es también de 5 logaritmos decimales.
Las normas EN 1276:2019 y EN 13727:2012+A2:2015 exigen una reducción de al menos 5 logaritmos decimales para aplicaciones generales, que incluyen la desinfección de superficies y otros usos no específicos para las manos. Sin embargo, para los productos destinados al lavado de manos, se requiere una reducción de 3 logaritmos decimales.
Por otra parte, los procedimientos de validación son esenciales para asegurar la reproducibilidad y fiabilidad de los ensayos. Todas las normas detallan métodos para la preparación de suspensiones de microorganismos, condiciones de incubación y cálculos necesarios para determinar la eficacia biocida. Los cálculos incluyen determinar el número de unidades formadoras de colonias (UFC) antes y después del tratamiento con el desinfectante.
Para ello, se utilizan métodos de dilución-neutralización y filtración sobre membrana para neutralizar y eliminar la actividad biocida antes de realizar los recuentos bacterianos. Estos procedimientos aseguran que los resultados del ensayo reflejen adecuadamente la efectividad del producto.
El método de dilución-neutralización implica diluir la muestra tratada con un neutralizador específico que detiene la acción biocida del desinfectante, permitiendo que se cuenten solo los microorganismos sobrevivientes. El método de filtración sobre membrana, por otro lado, implica filtrar la muestra tratada a través de una membrana que captura los microorganismos, seguido de un lavado con un líquido de aclarado que elimina cualquier residuo del desinfectante, permitiendo un recuento preciso de los microorganismos sobrevivientes.
Tabla Resumen Comparativa
| Aspecto | EN 1656:2019 | EN 1276:2019 | EN13727:2012+A2:2015 |
| Objetivo | Evaluación de actividad bactericida de productos desinfectantes y antisépticos | ||
| Tipo de Ensayo | Ensayo de suspensión | ||
| Campo de Aplicación | Área veterinaria | Alimentaria, industrial, doméstica, institucional | Área médica |
| Condiciones de Ensayo | Sucias de nivel bajo (3 g/l albúmina)
Sucias de nivel alto (10 g/l albúmina + 10 g/l extracto de levadura) |
Limpias (0,3 g/l albúmina)
Sucias (3 g/l albúmina) Leche (1% v/v) |
Limpias (0,3 g/l albúmina bovina) Sucias (3 g/l albúmina bovina + 3 ml/l eritrocitos) |
| Organismos de Ensayo | Desinfectantes de superficies
Pseudomonas aeruginosa, Staphylococcus aureus Enterococcus hirae, Proteus hauseri. Desinfectantes de pezones Escherichia coli, Staphylococcus aureus, Streptococcus uberis |
Pseudomonas aeruginosa, Escherichia coli, Staphylococcus aureus, Enterococcus hirae, Enterococcus faecium | |
| Organismos de Ensayo Adicionales | Se pueden ensayar organismos de ensayo adicionales | Salmonella typhimurium, Lactobacillus brevis, Enterobacter cloacae | Se pueden ensayar organismos de ensayo adicionales |
| Requisitos de Reducción Logarítmica | General: ≥ 5 log
Desinfectantes de pezones: ≥ 5 log |
General ≥ 5 log
Lavado de manos ≥ 3 log |
|
En resumen, las normas EN 1656:2019, EN 1276:2019 y EN 13727:2012+A2:2015 proporcionan un marco robusto para evaluar la eficacia de antisépticos y desinfectantes en diversas aplicaciones. Comprender las similitudes y diferencias entre estas normas es esencial para su correcta aplicación y para asegurar la seguridad y efectividad de los productos en diferentes contextos. La correcta implementación de estos estándares no solo garantiza la efectividad de los productos, sino que también protege la salud pública al asegurar que los desinfectantes y antisépticos utilizados en diferentes sectores sean adecuados para sus propósitos específicos.
¿Por qué elegir los ensayos de aptitud de SHAPYPRO?
Con más de 10 años de experiencia en la evaluación de la eficacia de productos desinfectantes, ofrecemos programas de ensayos de aptitud cumpliendo los requisitos de ISO/IEC 17043 conforme a los requisitos EN 14885:2022/AC:2023.
La amplitud de nuestros conocimientos nos permite ayudar a los clientes en el desarrollo de nuevos métodos y proyectos de I+D.
Hemos desarrollado programas de ensayo de aptitud bajo EN 1656:2019, EN 1276:2019 y EN 13727:2012+A2:2015 con anterioridad.
Somos fabricantes de jabón diluido blando necesario para ambos desarrollos.
Ofrecemos un ensayo de aptitud a medida.
Los ensayos se realizan siguiendo normas y directrices internacionales validadas.
¿Deseas obtener nuestra agenda a 5 años? ¡Escríbenos!


